Новый жидкий симбиотический биокомплекс в алгоритме восстановления микробиоценоза при хеликобактер-ассоциированных заболеваниях
Главная » Научные публикации » Новый жидкий симбиотический биокомплекс в алгоритме восстановления микробиоценоза при хеликобактер-ассоциированных заболеваниях
Микробиология и эпидемиология Вестник Нижегородского университета им. Н.И. Лобачевского, 2012, № 2 (3), с. 100-106
УДК 615.331 616.34-008.87
НОВЫЙ ЖИДКИЙ СИМБИОТИЧЕСКИЙ БИОКОМПЛЕКС В АЛГОРИТМЕ ВОССТАНОВЛЕНИЯ МИКРОБИОЦЕНОЗА ПРИ ХЕЛИКОБАКТЕР-АССОЦИИРОВАННЫХ ЗАБОЛЕВАНИЯХ
© 2012 г. И.В. Соловьева, И.В. Белова, А.Г. Тонтина, Г.И. Григорьева,
Т.П. Иванова, В.А. Жирнов
Нижегородский НИИ эпидемиологии и микробиологии им. И.Н. Блохиной
Поступила в редакцию 09.04.2012
Показана эффективность включения нового симбиотического комплекса в диету больных язвенной болезнью желудка и двенадцатиперстной кишки, ассоциированной с Н. pylori, в период обострения и реабилитации после ушивания перфоративных язв. Использование пробиотика способствует восстановлению микрофлоры толстой кишки, повышению эффективности эрадикации Н. pylori, снижению активности и выраженности воспалительных реакций в слизистых оболочках желудочно-кишечного тракта.
Ключевые слова: симбиотический биокомплекс, пробиотик, Н. pylori, микрофлора, дисбиоз, язвенная болезнь.
Введение
Ряд ученых рассматривают Helicobacter pylori как комменсала, эволюционировавшего вместе с человеком и сосуществующего с макроорганизмом. Но в определенных ситуациях Н. pylori переходит в статус паразита [1, 2]. Хеликобактериоз сопровождается нарушением иммунореактивности, антимикробной резистентности, метаболическими отклонениями, дисбиотическими изменениями в составе микрофлоры. При этом сложные процессы, происходящие в организме, не позволяют достоверно судить о первичности или вторичности дисбиоза в генезе хеликобактер- ассоциированных хронических воспалительных заболеваний верхних отделов пищеварительного тракта. Хеликобактериоз можно рассматривать как частный случай дисбиоза слизистой оболочки желудка. Но поскольку хеликобактерная инфекция обычно связана с определенным кругом заболеваний органов пищеварения, то у таких больных следует ожидать развития системного дисбиоза, включая нарушения микробиоценоза толстой кишки. Так, например, инфицирование макроорганизма Н. pylori и длительное его персистирование в организме человека как чужеродного агента нарушает эндоэкологию пищеварительной трубки и может рассматриваться в качестве фактора, инициирующего и усугубляющего нарушения микробиоценоза желудочно-кишечного тракта (ЖКТ), способствующего подавлению роста симбиотической микрофлоры (бифидобактерий, лактобацилл, бактероидов, кишечной палочки и др.) и последующей колонизации слизистой оболочки патогенными и условно-патогенными микроорганизмами. Массивная антихеликобактерная терапия, назначение нерациональных схем лечения, нарушение режима и укорочение сроков приема препаратов способствуют появлению антибиотикоустойчивых штаммов Н. pylori и сопровождаются развитием выраженных дисбиотических явлений, требующих коррекции [3-5]. В качестве средств, нормализующих микрофолору, используют препараты нормофлоры и, в частности, пробиотики на основе живых лактобацилл, так как в литературе имеются данные об антагонистической активности последних к Н. pylori [6, 7]. Кроме того, ряд как зарубежных, так и отечественных авторов отмечают, что оральное введение живых лактобацилл препятствует колонизации желудочного эпителия Н. pylori и выработке мощного медиатора воспаления интерлейкина 8 [8, 9]. Работы различных авторов свидетельствуют также о том, что применение различных штаммов лактобацилл и бифидобактерий как в схемах с антибиотиками, так и без них приводит к элиминации хеликобактерий из организма и выраженной клинической эффективности «экологической» терапии гастритов и дуоденитов [6, 10, 11]. При использовании пробиоти-ков в качестве лечебного питания в комплексе антихеликобактерной терапии отмечается положительная динамика восстановления кишечной микрофлоры (увеличение содержания в фекалиях лакто- и бифидофлоры, уменьшение условно-патогенных бактерий и т.д.), а также более быстрое улучшение клинического состояния больных (исчезновение болей в животе, уменьшение дуодено-гастрального рефлюкса и т.д.) [12].
Все вышесказанное не оставляет сомнений в целесообразности включения пробиотиков в диету при массивной комплексной антибиотико- и химиотерапии хеликобактер-ассоциированньгх заболеваний желудка и двенадцатиперстной кишки.
Цель настоящей работы - изучение эффективности использования нового жидкого симбиотического биокомплекса для восстановления микрофлоры при терапии хеликобактер-ассоциированной язвенной болезни двенадцатиперстной кишки в стадии обострения и в период реабилитации после ушивания перфоративных гастродуоденальных язв.
Экспериментальная часть
В качестве пробиотика был использован сконструированный в Нижегородском НИИ эпидемиологии и микробиологии им. И.Н. Блохиной новый жидкий шестикомпонентный симбиотический биокомплекс - бактериальный концентрат 3 штаммов лактобацилл видов L. Plantarum, L. fermentum и 3 штаммов бифидобакте-рий видов В. bifidum, В. longum (патент №2192269 от 03.07.2000), в 1 мл которого содержится 109-10" живых микробных клеток. В качестве основы пробиотика использован гидролизат обезжиренного молока, представляющий собой гипоаллергенный раствор аминокислот и простейших пептидов. Несомненным достоинством биокомплекса является то, что стартерные культуры образуют устойчивую систему, обладающую высоким антагонизмом по отношению к патогенным и условно-патогенным бактериям, а также недетерминированной плазмидами резистентностью к действию антибактериальных препаратов, применяемых в схемах эрадикации Н. pylori [13].
Больные основных групп получали пробио-тик однократно, за 30 минут до приема пищи в дозе 5 мл в течение 25 дней параллельно с эрадикационной терапией хеликобактер-ассоциированных заболеваний с учетом фармакокинетики антибактериальных средств. Предложенная схема основана на полученных ранее результатах по изучению антибиотикорезистентности штаммов-продуцентов, входящих в комплексный препарат. Рекомендовалось принимать симбиотик в тот момент, когда концентрация антихеликобактерных препаратов в крови была еще эффективна для элиминации Н. pylori, но уже не влияла на жизнеспособность пробиотических микроорганизмов. Например, если в схеме лечения присутствовал ампициллин, то, учитывая его воздействие на штаммы, пробиотик назначался в промежутке между приемами данного препарата (5-6 часов), то есть в 13-14 часов (антибиотики утром и вечером).
Всего в период обострения язвенной болезни двенадцатиперстной кишки обследованы 70 человек. Определение исходных показателей до лечения и контрольное обследование после окончания терапии проводилось по схеме: фиброгастродуоденоскопия (ФГДС), морфологический метод определения Н. pylori, исследование микробного состава фекалий. Контроль эрадикации проводился через 6 недель после окончания антихеликобактерной терапии с помощью уреазного теста «De-nol-test» в сочетании с морфологическим исследованием биоптатов с окраской по методу Романовского-Гимзы [14].
Поскольку больные ранее уже получали эрадикационную терапию, в качестве базисной использовалась квадросхема: омепразол 20 мг 2 раза в день и де-нол 240 мг 2 раза в день до приема пищи - 10 дней, флемоксин солютаб 1000 мг 2 раза в день и фуразолидон 200 мг 2 раза в день после приема пищи - 7 дней [3, 15].
Пациентов разделили на 2 группы: контрольную - 39 человек, получавших стандартную антихеликобактерную терапию и плацебо, и основную - 31 человек, получавших наряду с базисной терапией новый жидкий симбиотический биокомплекс.
Эффективность включения пробиотика в диетотерапию в комплексе санаторно-курортной реабилитации в ранний период после ушивания перфоративных язв желудка и двенадцатиперстной кишки проанализирована у 182 больных на 12±1.7 день после операции. Обследование проводилось по следующей схеме: до лечения - фиброгастродуоденоскопия у всех пациентов, частично определение наличия Н. pylori цитологическим методом мазков-отпечатков и методом ПЦР в желудочном соке, гистологическое исследование биоптатов, бактериологическое исследование фекалий; после лечения -ФГДС, изучение микрофлоры фекалий.
Комплекс базисного реабилитационного лечения включал диетотерапию по диете № 1 [16]; щадящий двигательный режим; занятия лечебной физкультурой; прием минеральной сульфатно-кальциево-магниевой воды «Горьковская № 2» за 90 минут до приема пищи; токи надтональной частоты на послеоперационный рубец для профилактики спаечного процесса; прием одного из антисекреторных препаратов: ранитидин в дозе 300 мг в сутки или фамоти-дин - 40 мг в сутки, или омепразол - 40 мг в сутки. При наличии Н. pylori больным назначали тройную эрадикационную терапию, включающую антисекреторный препарат в сочетании с амоксициллином (2000 мг в сутки) и метронидазолом (1000 мг в сутки) или фуразолидоном (400 мг в сутки) в течение 7 дней [15].
Пациенты были разделены на три группы: первую контрольную - 51 человек, которые получали базисную терапию в сочетании с природными факторами (грязелечение) и плацебо, вторую контрольную - 83 человека, получавших базисную терапию и плацебо, и основную, состоящую из 48 человек, получавших базисную терапию в сочетании с природными факторами и новый жидкий симбиотический биокомплекс.
Исследование микрофлоры толстой кишки проводилось в соответствии с Методическими указаниями «Бактериологическая диагностика дисбактериоза кишечника», по методу, разработанному Р.В. Эпштейн-Литвак и Ф.Л. Вильшанской и модифицированному в лаборатории ГНИИЭМ [17, 18]. Оценка результатов бактериологического исследования проводилась в соответствии с ОСТ 91500.11.0004-2003 [19].
Для клинического обследования больных применялись общепринятые стандартные методы [15].
Значимость различий результатов исследований оценивали по критерию Стьюдента с поправкой Бонферрони для множественных сравнений с контролем (уровень значимости р < < 0.01) [20].
Результаты и их обсуждение
В группе пациентов с обострением язвенной болезни двенадцатиперстной кишки у всех больных до лечения выявлялся Я. pylori со слабой степенью контаминации слизистой оболочки желудка (до 20 микробных клеток в поле зрения). У большинства больных клинически определялся гастрит слабой или умеренной активности, а по данным ФГДС выраженность воспалительных изменений антрального отдела желудка соответствовала умеренной или выраженной степени. В слизистой оболочке двенадцатиперстной кишки преобладал диффузный дуоденит 3-й степени у пациентов в обеих группах.
По результатам бактериологического исследования фекалий 70 пациентов, взятых под наблюдение, в микрофлоре толстой кишки с высокой частотой обнаруживались дисбиотические изменения у 70.9% обследованных, из них 29.1% составил компенсированный дисбиоз 1-й степени, 28.7% - субкомпенсированный дисбиоз 2-й степени и 42.2% - декомпенсированный дисбиоз 3-й степени; эубиоз выявлялся в 29.1 % случаев.
Дисбиотические нарушения проявлялись резким угнетением бифидо- и лактофлоры у 25.3% обследованных, отсутствием бифидобактерий у 8.3% пациентов, отсутствием латобацилл у 16.4% человек, дефицитом бифидобактерий (менее 106 КОЕ/г) у 21.3% больных, дефицитом лактобацилл (менее 106 КОЕ/г) у 17.5% обследованных и наличием условно-патогенных микроорганизмов, таких как S. aureus (16.4%), К. pneumoniae (25.2%), дрожжеподобные грибы рода Candida (21.3%), Enterobacterspp. (2.9%) и М. morganii (1.4%).
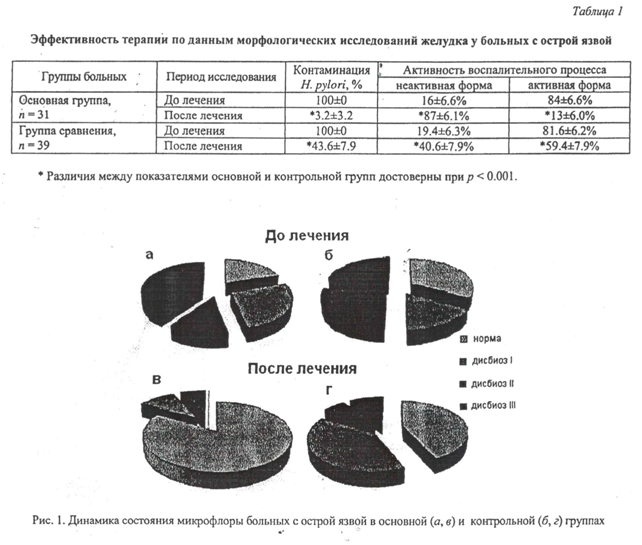
Через 6 недель после окончания антихеликобактерной терапии максимальная эрадикация Я. pylori у пациентов основной группы, получавших симбиотический биокомплекс, составила 96.8%, тогда как в контрольной группе - всего 56.4%. Активность антрум-гастрита снизилась у 96.6% пациентов основной группы против 65,6% контрольной. Выраженность гастрита снизилась у 93.5% против 71.9% контрольной группы. В основной группе дуоденит 3-й степени не определялся, тогда как в контрольной группе он был выявлен у 12.5% пациентов (табл. 1).
По микробиологическим данным через 6 недель после антихеликобактерной терапии в основной группе дисбиоз 3-й степени не диагностировался ни у одного больного, микрофлора полностью восстановилась у 83.3% получавших пробиотик, в то время как в контрольной группе у 10% пациентов после проведенного лечения было отмечено угнетение лакто- и бифидофлоры и диагностирован дисбиоз 3-й степени. Микрофлора нормализовалась только у 43.3% обследованных (рис. 1).
Таким образом, включение симбиотического биокомплекса в лечебные программы больным с обострением хеликобактер-ассоциированной язвенной болезни двенадцатиперстной кишки приводит к повышению эффективности терапии: существенно увеличивается частота эрадикации Я. pylori до 96.8% (р < 0.001), восстанавливается микрофлора толстой кишки до нормы у 83.3% пациентов и полностью устраняется декомпенсированный дисбиоз 3 степени (р< < 0.001). Снижается степень активности и тяжести гастрита и дуоденита.
В группе больных, находящихся на санаторно-курортной реабилитации в ранний период после ушивания перфоративных язв желудка и двенадцатиперстной кишки и обследованных до проведения курса реабилитационной терапии, Н. pylori обнаружен у 61.1% больных при цитологическом исследовании мазков-отпечатков и у 71% при использовании метода ПЦР. По данным ФГДС в 100% случаев отмечены рубцовые изменения луковицы двенадцатиперстной кишки или желудка, гастродуоденит разной степени активности зафиксирован у 94.4% обследованных, у 41.2% на фоне гастродуоденита выявлялись язвы желудка или двенадцатиперстной кишки, у 11.8% - эрозии слизистых. Бактериологическое исследование фекалий до лечения показало высокую частоту дисбиотических нарушений в обеих группах. Дисбиоз 2-й и 3-й степени отмечен у 89.5% пациентов.
Дисбиотические нарушения характеризовались резким угнетении лакто- и бифидофлоры в 16.7% случаев; отсутствием бифидобактерий у 20.8%, отсутствием лактофлоры у 25% обследованных; выявлением 5. epidermidis (25%), К. pneumoniae (41.7%), дрожжеподобных грибов рода Candida (12.5%), Enterobacter spp. (7%) и М. morganii (5.5%) в значимых количествах (105 и более КОЕ/г для УПМ и 104 и более КОЕ/г для Candida spp.
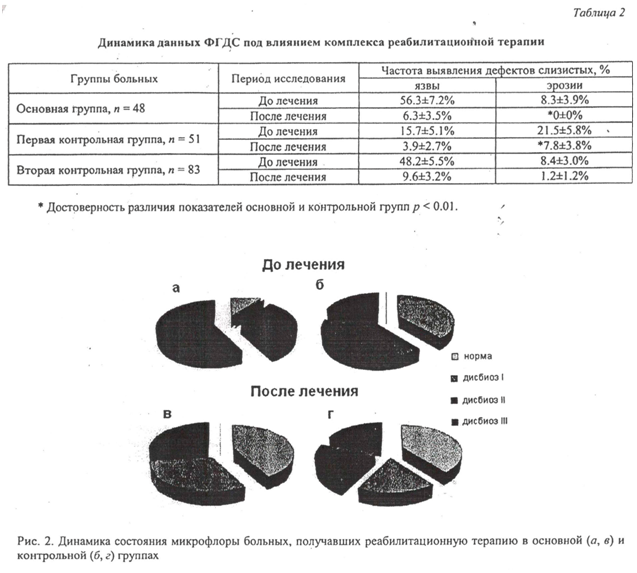
При обследовании через две недели после проведения курса лечения установлено, что под влиянием комплекса реабилитационных мероприятий произошло заживление язв в основной группе у 89±4.5% пациентов, эрозий у 100±0%. В первой группе сравнения (базис в сочетании с грязелечением) заживление язв отмечено у 80±5.6%, эрозий - у 85.7±4.9%. Во второй контрольной группе язвы зарубцевались у 75±4.8% больных, эрозии - у 63.3±5.3% (табл. 2).
В первой и второй контрольных группах выявлены вновь образовавшиеся язвы слизистых в 3.9±2.7% и 5±2.4% случаев, эрозии - в 3.9±2.7% и 4.8±2.3% случаев. В основной группе новые дефекты обнаружены не были (достоверность различия между группами 1и 3 р < 0.01).
По данным бактериологического исследования, проведенного после лечения, у всех пациентов основной группы отмечено улучшение микрофлоры. Дисбиоз 3-й степени не выявлен ни у одного человека, в то время как в контрольной группе в 20% случаев зафиксирован резко выраженный дисбиоз 3-й степени (рис. 2).
Полученные результаты свидетельствуют о том, что включение нового пробиотика в программы санаторно-реабилитационного лечения позволяет улучшить состояние микрофлоры толстой кишки, а также оказывает благоприятное влияние на клиническое течение основного заболевания у пациентов в ранний период после ушивания перфоративных язв желудка и двенадцатиперстной кишки.
Выводы
Таким образом, использование при терапии хеликобактер-ассоциированных заболеваний нового жидкого симбиотического биокомплекса в качестве специализированного продукта лечебного питания, как средства, нормализующего микрофлору кишечника, способствует эффективному восстанавлению эубиоза толстой кишки, повышает процент эрадикации Н. pylori, снижает активность и выраженность воспалительных изменений в слизистой оболочке желудка и двенадцатиперстной кишки. Включение его в программу реабилитационных мероприятий наряду с восстановлением микрофлоры улучшает качество жизни больных и сокращает восстановительный период лечения после ушивания перфоративных гастродуоденальных язв.
Список литературы
-
Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. М.: Триада-Х, 1998. С. 496.
-
Чернин В.В., Червинец В.М., Бондарен-ко В.М., Базлов С.Н. Язвенная болезнь, хронический гастрит и эзофагит в аспекте дисбактериоза эзофагогастродуоденальной зоны. Тверь: ООО «Изд-во «Триада», 2004. 200 с.
-
Маев И.В., Самсонов А.А., Голубев Н.Н. Лечение инфекции Helicobacter pylori // Фарматека. 2012. № 2 (235). С. 11-17.
-
Myllyoma Е. Effects of anti-h.pylori treatment and probiotic supplementation on intestinal microbiota // Int. J. Antimicrob. Agents. N 29 (1), P. 66-72.
-
Бондаренко B.M., Шапошникова Л.И. Клинический эффект жидких симбиотических биокомплексов, содержащих физиологически активные клетки бифидобактерий и лактобацилл. М.: Изд-во «Триада», 2007.95 с.
-
Бондаренко В.М., Воробьев А.А., Гершанович М.Л., Мельникова И.Ю., Петров Л.Н. Обоснование и тактика назначения в медицинской практике различных форм пробиотических препаратов // Сб. материалов международной конференции «Пробиотики, пребиотики, синбиотики и продукты функционального питания. Современное состояние и перспективы», Москва, 2-4 июня 2004. С. 5.
-
Coconnier М.-Н., Lievin V., Hemery Е., Ser-vin A.L. Antagonistic activity against helicobacter infection in vitro and in vivo by the Human Lactobacillus acidophilus Strain LB // Applied and Environmental Microbiology. 1998. V. 64. N. 11. P. 4573-4580.
-
Aiba Y., Suzuki N.. Kabir A.M., Takagi A., Koga Y. Lactic acid-rhediated suppressin of Helicobacter pylori by the oral administration of Lactobacillus salivarius as a probiotic in a gnotobiotic murin model // Am. J. Gastroenterol. 1998. V. 93. P. 2097-2101.
-
Marteau P.R., de Verse M., Cellier C.J. et al. Protection from gastrointestinal diseases with the use of probiotics // Am. J. Clin. Nutr. 2001. N 73 (2). P. 430-436.
-
Coconnier M.-H., Lievin V., Bernet-Camarad M.-F., Hudault S., Servin A.L. Antibacterial effects of adhering Human Lactobacillus acidophilus Strain LB // Antimicrobial Agents and Chemotherapy. 1997. V. 41. N 5. P. 1046-1052.
-
Gotteland M., Brunser O., Cruchet S. Systematic review: Are probiotics useful in controlling gastric colonization by Helicobacter pylori? // Aliment. Pharmacol. Ther. 2006. N 23 (8). P. 1077-1086.
-
Верткин А.Л., Артамонов B.E., Багатурия И.Ф., Машарова А.А., Габуева-Джипсаева Ж.В. Дисбактериоз кишечника, как побочный эффект антихеликобактерной терапии и новый способ его коррекции // Медицинская картотека. 1998. № 10. С. 21-23.
-
Патент РФ № 2184555. Способ лечения язвенной болезни • двенадцатиперстной кишки / Яковлев М.Г., Кузин В.Б., Дугина В.В., Потехин П.П., Соколова К.Я., Соловьева И.В. (Россия). Заявка №2000121246/14 от 07.08.2000; опубл. 10.07.2002, Бюл. № 9.
-
Исаков В.А., Домарадский И.В. Хеликобактериоз. М.: ИД Медпрактика, 2003.412 с.
-
Стандарты диагностики и лечения кислотозависимых и ассоциированных с Helicobacter pylori заболеваний (4-е Московское соглашение) приняты X съездом НОГР 5 марта 2010 года // Экспериментальная и клиническая гастроэнтерология. 2010. № 5. С. 113-118.
-
Барановский А.Ю., Назаренко Л.И. Основы питания россиян: Справочник. СПб.: Питер, 2007. 528 с.
-
Эпштейн-Литвак Р.В., Вильшанская Ф.Л. Бактериологическая диагностика дисбактериоза кишечника // Методические материалы. М., 1969. 23 с.
-
Эпштейн-Литвак Р.В. и др. Бактериологическая диагностика, дисбактериоза. Методические рекомендации. М., 1.977. 20 с.
-
ОСТ 91500.11.0004-2003. Протокол ведения больных. Дисбактериоз кишечника. Утвержден приказом МЗ РФ № 231 от 09.06.2003. Москва, 2003. 173 с.
-
Сергиенко В.И., Бондарева И.Б. Математическая статистика в клинических исследованиях. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа, 2006.304 с.